A tecnoloxía de diagnóstico molecular utiliza métodos de bioloxía molecular para detectar a expresión e estrutura do material xenético do corpo humano e varios patóxenos, co fin de acadar o propósito de predicir e diagnosticar enfermidades.
Nos últimos anos, coa actualización e iteración da tecnoloxía de diagnóstico molecular, a aplicación clínica do diagnóstico molecular fíxose cada vez máis extensa e profunda, e o mercado de diagnóstico molecular entrou nun período de rápido desenvolvemento.
O autor resume as tecnoloxías de diagnóstico molecular comúns no mercado e divídese en tres partes: a primeira parte presenta a tecnoloxía PCR, a segunda parte a tecnoloxía de amplificación isotérmica de ácidos nucleicos e a segunda parte a tecnoloxía de secuenciación.
01
Parte I: Tecnoloxía PCR
Tecnoloxía PCR
A PCR (reacción en cadea da polimerase) é unha das tecnoloxías de amplificación de ADN in vitro, cunha historia de máis de 30 anos.
A tecnoloxía PCR foi pioneira en 1983 por Kary Mullis de Cetus, EUA.Mullis solicitou unha patente de PCR en 1985 e publicou o primeiro traballo académico de PCR sobre Science no mesmo ano.Mullis gañou o Premio Nobel de Química en 1993.
Principios básicos da PCR
A PCR pode amplificar fragmentos de ADN obxectivo máis dun millón de veces.O principio é que baixo a catálise da ADN polimerase utilízase a cadea de ADN nai como molde e un cebador específico úsase como punto de partida para a extensión.Replícase in vitro mediante etapas como a desnaturalización, o recocido e a extensión.O proceso do ADN da cadea filla complementario ao ADN molde da cadea nai.
O proceso estándar de PCR divídese en tres pasos:
1. Desnaturalización: utiliza alta temperatura para separar as dobres cadeas de ADN.Os enlaces de hidróxeno entre as dobres cadeas de ADN rómpese a altas temperaturas (93-98 °C).
2. Recocido: despois de separar o ADN de dobre cadea, a temperatura redúcese para que o cebador poida unirse ao ADN monocatenario.
3. Extensión: a ADN polimerase comeza a sintetizar cadeas complementarias ao longo das cadeas de ADN a partir dos cebadores unidos cando a temperatura baixa.Cando se completa a extensión, complétase un ciclo e o número de fragmentos de ADN duplícase.
Ao alternar estes tres pasos 25-35 veces, o número de fragmentos de ADN aumentará exponencialmente.
O enxeño da PCR é que se poden deseñar diferentes cebadores para diferentes xenes diana, de xeito que os fragmentos do xene diana poden ser amplificados nun curto período de tempo.
Ata agora, a PCR pódese dividir en tres categorías, a saber, PCR ordinaria, PCR cuantitativa fluorescente e PCR dixital.
A primeira xeración de PCR ordinaria
Use un instrumento de amplificación PCR común para amplificar o xene diana e, a continuación, use electroforese en xel de agarosa para detectar o produto, só se pode facer análise cualitativa.
As principais desvantaxes da PCR de primeira xeración:
-Propenso a amplificación inespecífica e resultados falsos positivos.
-A detección leva moito tempo e o funcionamento é engorroso.
-Só se poden facer probas cualitativas.
PCR cuantitativa de fluorescencia de segunda xeración
A PCR cuantitativa de fluorescencia (PCR en tempo real), tamén coñecida como qPCR, úsase para controlar a acumulación de produtos amplificados mediante a acumulación de sinais fluorescentes engadindo sondas fluorescentes que poden indicar o progreso do sistema de reacción, e para xulgar os resultados a través da curva de fluorescencia, e pódese cuantificar coa axuda do valor Cq e da curva estándar.
Dado que a tecnoloxía qPCR lévase a cabo nun sistema pechado, a probabilidade de contaminación redúcese e o sinal de fluorescencia pódese controlar para a detección cuantitativa, polo que é a máis utilizada na práctica clínica e converteuse na tecnoloxía dominante na PCR.
As substancias fluorescentes utilizadas na PCR cuantitativa fluorescente en tempo real pódense dividir en: sondas fluorescentes TaqMan, balizas moleculares e colorantes fluorescentes.
1) Sonda fluorescente TaqMan:
Durante a amplificación por PCR, engádese unha sonda fluorescente específica mentres se engade un par de cebadores.A sonda é un oligonucleótido, e os dous extremos están marcados respectivamente cun grupo fluorescente indicador e un grupo fluorescente extintor.
Cando a sonda está intacta, o sinal fluorescente emitido polo grupo informador é absorbido polo grupo de extinción;durante a amplificación da PCR, a actividade exonuclease 5′-3′ do encima Taq escinde e degrada a sonda, facendo que o grupo fluorescente informador e o extinguidor sepárase o grupo fluorescente, de xeito que o sistema de monitorización da fluorescencia pode recibir o sinal de fluorescencia, é dicir, cada vez que se amplifica unha cadea de ADN, o sinal de fluorescencia acumúlase completamente e acumúlase a formación de fluorescencia. o produto PCR.
2) Colorantes fluorescentes SYBR:
No sistema de reacción PCR, engádese un exceso de colorante fluorescente SYBR.Despois de que o colorante fluorescente SYBR se incorpore de forma non específica á dobre cadea de ADN, emite un sinal fluorescente.A molécula de colorante SYBR que non está incorporada á cadea non emitirá ningún sinal fluorescente, garantindo así o sinal fluorescente. O aumento dos produtos da PCR está completamente sincronizado co aumento dos produtos da PCR.SYBR só se une ao ADN de dobre cadea, polo que a curva de fusión pódese usar para determinar se a reacción de PCR é específica.
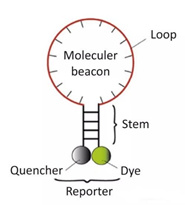
3) Faros moleculares
É unha sonda de oligonucleótido dobre marcado con bucle de talo que forma unha estrutura de forquilla dunhas 8 bases nos extremos 5 e 3.As secuencias de ácidos nucleicos en ambos os extremos están emparelladas complementariamente, o que fai que o grupo fluorescente e o grupo de extinción estean axustados.Cerca, non producirá fluorescencia.
Despois de xerar o produto da PCR, durante o proceso de recocido, a parte media da baliza molecular emparellase cunha secuencia de ADN específica e o xene fluorescente sepárase do xene quencher para producir fluorescencia.
As principais desvantaxes da PCR de segunda xeración:
Aínda falta sensibilidade e a detección de exemplares de pouca copia non é precisa.
Hai unha influencia do valor de fondo e o resultado é susceptible de interferencias.
PCR dixital de terceira xeración
A PCR dixital (DigitalPCR, dPCR, Dig-PCR) calcula o número de copia da secuencia de destino mediante a detección do punto final e pode realizar unha detección cuantitativa absoluta precisa sen utilizar controis internos e curvas estándar.
A PCR dixital usa a detección do punto final e non depende do valor Ct (limiar do ciclo), polo que a reacción da PCR dixital vese menos afectada pola eficiencia da amplificación e mellórase a tolerancia aos inhibidores da reacción de PCR, cunha alta precisión e reproducibilidade.
Debido ás características de alta sensibilidade e alta precisión, non é facilmente interferido polos inhibidores da reacción de PCR, e pode lograr unha verdadeira cuantificación absoluta sen produtos estándar, que se converteu nun punto de investigación e aplicación.
Segundo as diferentes formas da unidade de reacción, pódese dividir en tres tipos: sistemas microfluídicos, chip e gotas.
Hora de publicación: 08-07-2021