A vacina de ARNm de Pfizer contra o COVID reavivou a paixón por usar o ácido ribonucleico (ARN) como obxectivo terapéutico.Non obstante, dirixir o ARN con moléculas pequenas é moi difícil.
O ARN só ten catro bloques de construción: adenina (A), citosina (C), guanina (G) e uracilo (U) que substitúe a timina (T) que se atopa no ADN.Isto fai que a selectividade das drogas sexa un obstáculo case insuperable.Pola contra, hai 22 aminoácidos naturais que compoñen as proteínas, o que explica por que a maioría dos fármacos orientados a proteínas teñen unha selectividade relativamente boa.
Estrutura e función do ARN
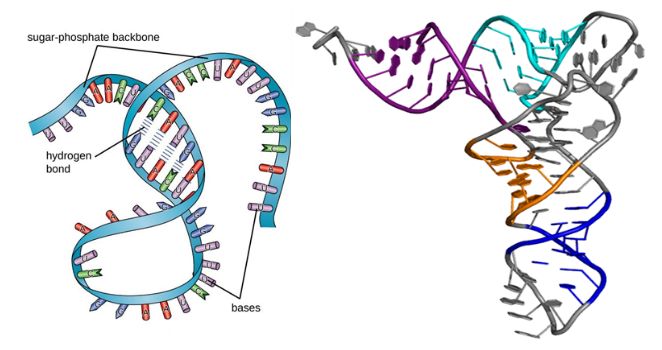
Como as proteínas, as moléculas de ARN teñen estruturas secundarias e terciarias, como se mostra na figura seguinte.Aínda que son macromoléculas de cadea única, a súa estrutura secundaria toma forma cando o emparellamento de bases provoca protuberancias, bucles e hélices.Despois, o pregamento tridimensional conduce á estrutura terciaria do ARN, que é esencial para a súa estabilidade e función.
Figura 1. Estrutura do ARN
Hai tres tipos de ARN:
- ARN mensaxeiro (ARNm)transcribe a información xenética do ADN e transfírese como unha secuencia de bases ao ribosoma;l
- ARN ribosómico (ARNr)forma parte dos orgánulos sintetizadores de proteínas chamados ribosomas, que se exportan ao citoplasma e axudan a traducir a información do ARNm en proteínas;
- ARN de transferencia (ARNt)é o enlace entre o ARNm e a cadea de aminoácidos que forma a proteína.
Dirixirse ao ARN como diana terapéutica é moi atractivo.Descubriuse que só o 1,5% do noso xenoma se traduce finalmente en proteínas, mentres que o 70%-90% transcríbese a ARN.As moléculas de ARN son as máis importantes para todos os organismos vivos.Segundo o "dogma central" de Francis Crick, o papel máis crítico do ARN é traducir a información xenética do ADN a proteínas.Ademais, as moléculas de ARN tamén teñen outras funcións, incluíndo:
- Actuando como moléculas adaptadoras na síntese de proteínas;l
- Serve como mensaxeiro entre o ADN e o ribosoma;l
- Son portadores de información xenética en todas as células vivas;l
- Promover a selección ribosómica dos aminoácidos correctos, necesario para sintetizar novas proteínasin vivo.
Antibióticos
A pesar de ser descuberto xa na década de 1940, o mecanismo de acción de moitos antibióticos non foi dilucido ata finais dos anos 80.Descubriuse que unha gran proporción de antibióticos actúan uníndose aos ribosomas bacterianos para evitar que fagan proteínas apropiadas, matando así as bacterias.
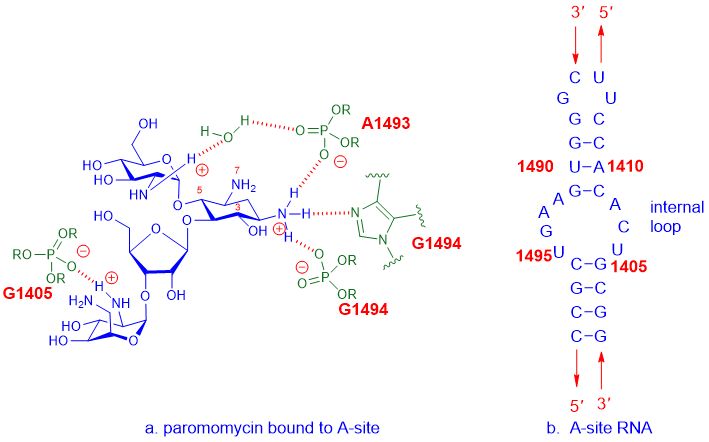
Por exemplo, os antibióticos aminoglucósidos únense ao sitio A do ARNr 16S, que forma parte da subunidade do ribosoma 30S, e despois interfiren coa síntese de proteínas para interferir co crecemento bacteriano, o que finalmente leva á morte celular.O sitio A refírese ao sitio aminoacilo, tamén coñecido como o sitio aceptor do ARNt.A interacción detallada entre fármacos aminoglicósidos, comoparomomicina, e o sitio A deE. coliO ARN móstrase a continuación.
Figura 2. A interacción entre a paromomicina e o sitio A deE. coliARN
Desafortunadamente, moitos inhibidores do sitio A, incluídos os fármacos aminoglucósidos, teñen problemas de seguridade como a nefrotoxicidade, a ototoxicidade específica e irreversible dependente da dose.Estas toxicidades son o resultado da falta de selectividade dos fármacos aminoglucósidos para recoñecer pequenas moléculas de ARN.
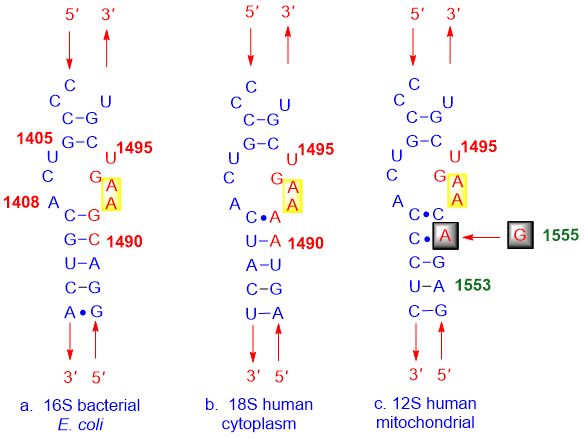
Como se mostra na seguinte figura: (a) a estrutura das bacterias, (b) a membrana celular humana e (c) o sitio A mitocondrial humano son moi similares, polo que os inhibidores do sitio A se unen a todos eles.
Figura 3. A unión non selectiva do inhibidor do sitio A
Os antibióticos de tetraciclina tamén inhiben o sitio A do ARNr.Inhiben selectivamente a síntese de proteínas bacterianas uníndose de forma reversible a unha rexión helicoidal (H34) na subunidade 30S complexada con Mg.2+.
Por outra banda, os antibióticos macrólidos únense preto do sitio de saída (sitio E) do túnel dos ribosomas bacterianos para os péptidos nacientes (NPET) e bloquealo parcialmente, inhibindo así a síntese de proteínas bacterianas.Por último, antibióticos oxazolidinona comolinezolid(Zyvox) únense a unha fenda profunda da subunidade ribosomal bacteriana 50S, que está rodeada por nucleótidos de ARNr 23S.
Oligonucleótidos antisentido (ASO)
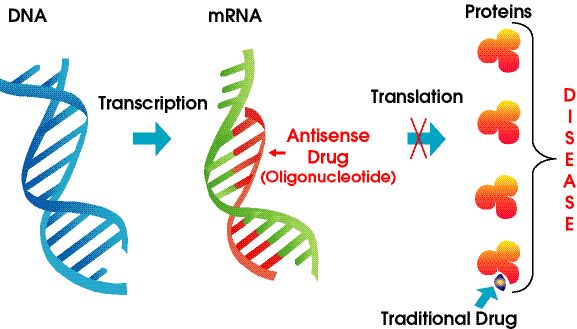
Os fármacos antisentido son polímeros de ácidos nucleicos modificados químicamente que teñen como obxectivo o ARN.Dependen do emparellamento de bases Watson-Crick para unirse ao ARNm diana, o que produce silenciamento xenético, bloqueo estérico ou alteración do empalme.Os ASO poden interactuar con pre-ARN no núcleo celular e ARNm maduros no citoplasma.Poden dirixirse a exóns, intróns e rexións non traducidas (UTR).Ata a data, máis dunha ducia de medicamentos ASO foron aprobados pola FDA.
Figura 4. Tecnoloxía antisentido
Fármacos de pequenas moléculas dirixidos ao ARN
En 2015, Novartis informou de que descubriran un regulador de splicing SMN2 chamado Branaplam, que mellora a asociación de U1-pre-ARNm e rescata ratos SMA.
Por outra banda, o Risdiplam de PTC/Roche (Evrysdi) foi aprobado pola FDA en 2020 para o tratamento da SMA.Do mesmo xeito que Branaplam, Risdiplam tamén funciona regulando o empalme dos xenes SMN2 relevantes para producir proteínas SMN funcionais.
Degradadores de ARN
RBM significa RNA-binding motif protein.Esencialmente, a indol sulfonamida é un adhesivo molecular.Recluta selectivamente RBM39 para a ubiquitina ligase CRL4-DCAF15 E3, promovendo a poliubiquitinación de RBM39 e a degradación das proteínas.O esgotamento xenético ou a degradación mediada por sulfonamida de RBM39 induce anomalías significativas de empalme en todo o xenoma, que finalmente conducen á morte celular.
Os ARN-PROTAC desenvólvense para degradar as proteínas de unión ao ARN (RBP).PROTAC usa un enlazador para conectar o ligando da ligase E3 ao ligando de ARN, que se une ao ARN e ás RBP.Dado que a RBP contén dominios estruturais que poden unirse a secuencias de oligonucleótidos específicas, RNA-PROTAC usa unha secuencia de oligonucleótidos como ligando para a proteína de interese (POI).O resultado final é a degradación dos RBP.
Recentemente, o profesor Matthew Disney da Scripps Institution of Oceanography inventou o ARNquimeras orientadas á ribonuclease (RiboTAC).RiboTAC é unha molécula heterofuncional que conecta un ligando RNase L e un ligando de ARN cun enlazador.Pode recrutar específicamente a RNase L endóxena para dianas específicas de ARN e despois eliminar con éxito o ARN mediante o mecanismo de degradación do ácido nucleico celular (RNase L).
A medida que os investigadores aprendan máis sobre a interacción entre moléculas pequenas e dianas de ARN, no futuro xurdirán máis fármacos que utilicen este método.
Hora de publicación: 02-ago-2023